特集2 パーキンソン病 薬とリハビリで進行を防ぐ
 |
| 川上明男 新潟・下越病院 (神経内科) |
めざましく進歩してきた研究と治療
パーキンソン病は、1817年にイギリスのジェームズ・パーキンソンが「振戦麻痺」として報告したのが始まりです。振戦麻痺とは、手指の震えや手足・身体の麻痺のことで、特徴的な症状です。
パーキンソン病は、アルツハイマーと同じく脳の神経細胞が徐々に減少する病気の一つで、少しずつ全身の運動障害が進みます。進行すると自律神経の障害や認知症が起きることがあります。
発症率は、人口10万人あたり100~150人、60歳以上では100人に1人くらいです。中年以降に発症し加齢とともに増加します。また5%ほどの患者さんでは遺伝が関係しています。
4大症状
体がうまく動かなくなる
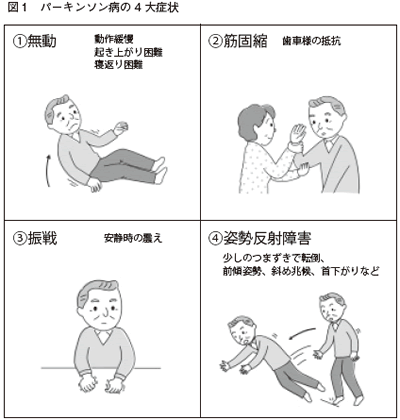
運動機能の障害では4つの大きな症状があります。(1)無動(動きがのろい、動けない)、(2)筋固縮(手足の筋肉がこわばって、動かすとカクカクと歯 車のような抵抗がある)、(3)振戦(手足が震える)、(4)姿勢反射障害(押されるとバランスを崩し立ち直れない)(図1)。多くは左右のどちらかに強く現れます。
ほかには、▽顔の表情がなくなる(仮面様顔貌)、▽小刻み歩行、▽歩行時のすくみ、▽前傾姿勢、▽言語障害(小声、抑揚がなくなる)などの症状があります。
病気の進行とともに寝返りや起き上がり、起立、歩行が困難になり、転倒、嚥下障害(飲み込み困難)などが起きます。
体の動き以外では、消化管や血管の働きを調節する自律神経の障害により、便秘、起立性低血圧、多汗などの症状が出たり、精神障害(抑うつ、幻視、認知症など)や嗅覚障害などが起きることがあります。
 |
病気の起こり方
ドパミンの減少が関係
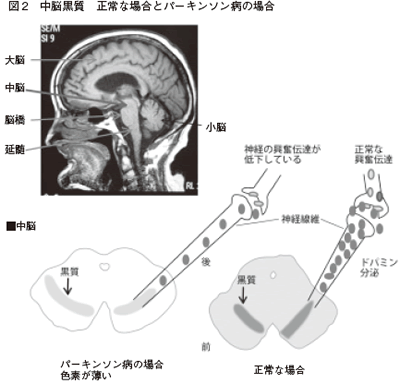
パーキンソン病の発症には、「ドパミン」という神経伝達物質の減少が関わっています。大脳の下にある中脳には、色素が沈着した「黒質」という部分があり、ここで、ドパミンがつくられます。
ドパミンが神経線維を通って「線条体」に送られると、運動を調節する刺激が出ます。これを受けた「大脳皮質」が全身の筋肉に運動の指令を出すことで、私 たちは自分の体を思うように動かすこと(随意運動)ができるのです。
パーキンソン病では、黒質のドパミン産生細胞が減少してドパミンが枯渇し、運動を調整する刺激が低下するため、自由に体を動かすことが困難になってくるわけです(図2)。
黒質を顕微鏡で見ると、正常な脳組織にはない「レビー小体」という物質がたまっていることがわかります。このレビー小体が黒質に作用して、ドパミン産生細胞を減らしていると考えられています。
 |
■レビー小体
レビー小体はなかなかの悪者で、自律神経にたまると自律神経障害を起こし、海馬や大脳皮質にたまると認知症を、嗅覚神経にたまるとにおいの障害を引き起こすことがわかっています。
さらにレビー小体の中には、α─シヌクレインという物質が蓄積していることがわかりました。α─シヌクレインは凝り固まると神経に対する毒性があると考 えられています。また、病的なα─シヌクレインは、一度生じるとどんどん増え続けるという説があります。
しかしこの物質がたまってくるそもそもの原因は、よくわかっていません。
30年ほど前、合成麻薬であるMPTPという物質が黒質にたまり、パーキンソン病と似た状態になったという報告がありました。α─シヌクレインの蓄積に は、加齢や遺伝のほか、農薬や銅・マンガン・鉛・鉄の過剰摂取、また食事なども関係しているのではないかと考えられています。
診断の方法
レボドパで改善されれば
パーキンソン病のそもそもの原因はわかっていませんが、症状を改善する薬が、40年以上前からあります。レボドパ(L─ドーパ)という薬で、これを飲むと、脳内でドパミンに変換され、不足を補ってくれるのです。
ですから、パーキンソン病の診断にもこれが使われます。4大症状のうちのいくつかが認められ、レボドパの服用で症状が改善すればパーキンソン病と診断で きます。もちろん他の病気ではないことも確認します。さらに4大症状のうち、「無動」を含む2つ以上の症状が認められるものをパーキンソン症候群と呼んで います。
パーキンソン症候群には、パーキンソン病も含まれますが、他の病気も含まれます。(1)脳血管障害(多発性脳梗塞などによるもの)、(2)多系統萎縮 症、(3)進行性核上性麻痺、(4)皮質基底核変性症、(5)正常圧水頭症、(6)薬剤の副作用(ある種の抗精神薬による)、(7)マンガン中毒、(8) 脳炎後、(9)一酸化炭素中毒などです。
多くはレボドパが効かず、症状のうち、しばしば「振戦」がありません。逆に丸薬を丸めるような振戦を静止時に認めるときはパーキンソン病が多いようです。
パーキンソン病と類似疾患は鑑別が困難なことが多いのですが、脳のCTやMRI画像が鑑別に役立つことがあります。
パーキンソン病は正常画像で特徴的な所見はありませんが、類似疾患では脳出血や梗塞、大脳皮質の萎縮など、画像で異常が発見されることがよくあります。
また、パーキンソン病で心臓の交感神経が障害されることから、MIBG心筋シンチグラムという検査で鑑別診断することもあります。認知症を伴ったパーキ ンソン病の場合、脳血流スペクト検査をすると、かなりの確率で後頭葉の血流低下があることが認められます。
治療
薬(レボドパ)を中心に
治療の中心は薬です。ほかに脳深部刺激療法、リハビリテーションなどがあります。
薬物治療の主要な柱はレボドパ(メネシットやEC─ドパール、ネオドパストンなど)です。レボドパはパーキンソン病の症状を最もよく改善させますが、症 状が進むと、服用後2?3時間で効果が薄れるようになったり、手足が勝手に動く不随意運動がでてきたりすることがあります。まれに消化器症状がでます。
こうした欠点を補うことを目的に、レボドパよりやや弱いものの、類似の作用を持つドパミン受容体刺激薬(レキップ、ビシフロール、ペルマックス、カバ サールなど)が開発されました。副作用として、眠気、幻覚や、まれに心臓弁膜症などがあります。
ほかに、▽ドパミンの分解を抑え濃度を上げるMAO─B阻害薬(セレギリン)、▽レボドパの作用時間を延長させるCOMT阻害薬(コムタン)、▽ドパミ ンの合成・放出を促すアマンタジン(シンメトレル)、▽ドパミンと拮抗するアセチルコリンの作用を弱めることによって症状を改善する抗コリン薬(アーテ ン、アキネトン)などがあります。
すくみ足や起立性低血圧にドロキシドパ(ドプス)なども使われます。
脳深部刺激療法は、脳深部の神経核に電極を植え込み、弱い電気刺激をおこなって筋固縮や無動・振戦を改善する治療です。病気が進行し薬物治療が難しくなっ てきた患者さんに実施されることがあります。
リハビリ
体を動かすことが大切
リハビリテーションは、薬物療法と並行しておこないます。
全身の緊張をときほぐし、筋肉の柔軟性を高めるリラクゼーションとストレッチ、手足の関節を最大限動かす練習、頸部や体幹をねじる運動、起き上がりや立 ち上がり、歩行、とりわけ音リズムや音楽に合わせた歩行などが大切です。
パーキンソン病では足がすくみ前に出なくなることがよくあります。狭い所の歩行や、方向転換するときに目立ちます。ところが逆に、足元に障害物があると すくんだ足がすーっと前に伸びて障害物をまたげたり、平地を歩くよりも階段が上りやすいことがあります(逆説歩行)。この特徴を利用して、床にテープなど で等間隔のラインを作ると視覚刺激に訴え、歩行に良い場合があります。
小声や抑揚の欠けた会話、不明瞭な会話に対しては、発声練習をおこないます。嚥下障害にも食材を工夫しながら飲み込みの練習をおこないます。
進行した場合は
特定疾患申請や身障者手帳も
パーキンソン病の根本原因はまだよくわかっていません。治療は症状をある程度改善しますが、病気の進行を止めることはできません。数年単位で進行していくのが普通です。
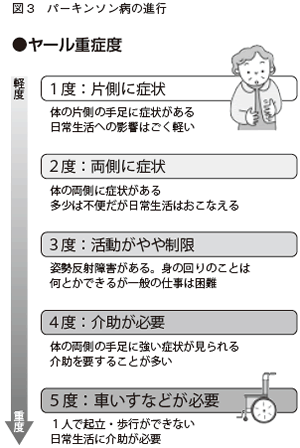
パーキンソン病の重症度はヤール分類(図3)がよく用いられます。発症後10年ほど経つとほとんどステージ3(身の回りのことが何とかできるが、一般の仕事は困難、姿勢反射に障害がみられる)となります。起き上がりや起立歩行に時間がかかり転倒することがあります。
また薬の有効な時間と切れる時間とが現れ、薬を何回も服用せざるをえない場合もあります。まれに不随意運動が出現します。
15年ほどすると、物忘れ、場所がわからない、注意力低下、物事の処理ができないなど認知症の症状が現れることがあります。しばしば、人や虫が見える幻 視が出現します。嚥下障害が出て誤嚥性肺炎の原因となります。起立性低血圧が悪化し起立時の失神発作や、入浴時の血圧低下などを生じることがあります。
新薬も開発されているので、多くの薬を組み合わせて服用する、またリハビリをおこなうことで症状の改善をはかることが大切です。杖や歩行器、車いすなど の使用や、家にベッドを入れて手すりをつける、トイレの改修など環境改善も重要です。パーキンソン病の場合は40才以上が介護保険制度の対象となります。 介護サービスの利用も検討しましょう。
パーキンソン病の薬は高額です。重症度でステージ3以上のときは「特定疾患申請」が可能となります。特定疾患の対象に認定されると、薬や医療費に一部公的補助がでます。
また起立、歩行障害で転倒しやすくなると身体障害者手帳の2級や3級に該当します。こちらも検討しましょう。
 |
めざましい進歩
iPS細胞で臨床治験開始
パーキンソン病の研究・治療は、1969年レボドパの投薬成功から45年が経過し、めざましい進歩をとげました。今後、病気発症の遺伝子やα─シヌクレインの研究で根本原因が解明され、根治が可能な日もやってくると思われます。
将来の治療として期待されているものに、遺伝子治療とES細胞、iPS細胞の利用があります。遺伝子を使ってドパミン産生をおこなう研究や神経細胞の脱 落を防ぐ研究などがおこなわれています。またES細胞、iPS細胞など幹細胞(万能細胞)からドパミン神経細胞を分化させる研究もおこなわれています。
最近、京都大学でiPS細胞を使ったパーキンソン病臨床治験を開始するとの報道がされました。今後の成果が期待されます。
いつでも元気 2014.5 No.271





